Phần trăm về khối lượng của oxi cao nhất trong oxit nào cho dưới đây?
Bài 1: Phần trăm về khối lượng của oxi cao nhất trong oxit nào cho dưới đây?
A. CuO B. ZnO C. FeO D. CaO
Bài 2: Oxit có của 1 NTố có hóa trị III chứa 30 % oxi về khối lượng. CTHH của oxit đó là:
A. Fe2O3 B. Al2O3 C. Cr2O3 D. N2O3
Bài 3: Đốt hòan toàn hỗn hợp 5,6g cacbon và lưu huỳnh cần 6,72 lít khí oxi (đktc).
a. Viết PTHH.
b. Tính khối lượng mỗi chất có trong hỗn hợp ban đầu.
Bài 4: Có 3 lọ thủy tinh đựng riêng biệt 3 khí : oxi, không khí, cacbonic được đây kín. Bằng phương pháp hóa học hãy nhận biết các chất khí trên?
Bài 5: Cho 6,5g Zn hòa tan vào dd chứa 0,2mol H2SO4 .
a. Viết PTHH minh họa.
b. Chất nào dư? Khối lượng là bao nhiêu?
c. Tính thể tích khí H2 thu được (đktc)?
Bài 6: Dùng H2 để khử 50g hỗn hợp CuO và Fe2O3, trong đó Fe2O3 chiếm 80% khối lượng hỗn hợp.
a. Viết PTHH.
b. Tính khối lượng mỗi kim loại thu được.
c. Tính thể tích khí H2 cần dùng.
Bài 7: Đốt cháy hoàn toàn 5,4 gam Al trong không khí, thu được chất rắn là Al2O3
a. Viết phương trình phản ứng xảy ra và tính khối lượng Al2O3 tạo thành
b. Tính thể tích không khí cần dùng (biết rằng Oxi chiếm 20% không khí) (các thể tích đo ở đktc)
Bài 8: Đốt cháy hoàn toàn 3,9 gam một kim loại M hóa trị I thu được 4,7 gam một oxit A.
a. Cho biết A thuộc loại oxit nào? Vì sao?
b. Tìm tên kim loại M và cho biết bazơ tương ứng của oxit A
Bài 9: Đốt cháy hoàn toàn 13,8 gam hỗn hợp gồm Al và Fe, thu được 21,8 gam hỗn hợp 2 oxit Al2O3 và Fe3O4
a. Viết các phản ứng xảy ra
b. Tính thể tích không khí cần dùng để đốt cháy hoàn toàn hỗn hợp 2 kim loại trên? (các thể tích đo ở đktc)
Bài 10: Viết các phương trình phản ứng biểu diễn sự oxi hoá các chất sau:
a.Mg
b. H2
c. Al
d. Zn
Biết sản phẩm cháy lần lượt có công thức là: MgO, H2O, Al2O3, ZnO.
Bài 11: Nung nóng kali clorat KClO3 thu được 3,36 lít khí oxi (đktc)
a. Viết phương trình phản ứng
b. Tính khối lượng KClO3 cần dùng.
Bài 12: Đốt cháy hoàn toàn 1,86g sắt ở nhiệt độ cao .
a. Tính khối lượng oxit sắt thu được sau phản ứng.
b. Tính thề tích khí oxi cần dùng (đktc).
c. Tính thể tích không khí cần thiết để có đủ lượng oxi trên.
Trang chủ
Giải bài tập Online
Đấu trường tri thức
Dịch thuật
Flashcard - Học & Chơi
Cộng đồng
Trắc nghiệm tri thức
Khảo sát ý kiến
Hỏi đáp tổng hợp
Đố vui
Đuổi hình bắt chữ
Quà tặng và trang trí
Truyện
Thơ văn danh ngôn
Xem lịch
Ca dao tục ngữ
Xem ảnh
Bản tin hướng nghiệp
Chia sẻ hàng ngày
Bảng xếp hạng
Bảng Huy hiệu
LIVE trực tuyến
Đề thi, kiểm tra, tài liệu học tập




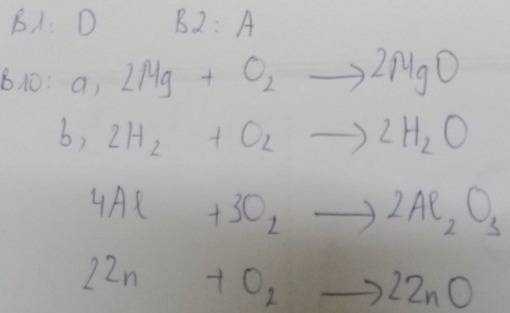


 Trả lời nhanh trong
Trả lời nhanh trong 



 Xem thêm
Xem thêm  Thưởng th.2.2025
Thưởng th.2.2025 Bảng xếp hạng
Bảng xếp hạng