Chào bạn, tôi sẽ giúp bạn giải bài tập này.
Tóm tắt đề bài:
- Hòa tan 36g oxit kim loại M (hóa trị II) vào dung dịch H2SO4 20% (loãng) vừa đủ.
- Dung dịch thu được có nồng độ 28,07%.
- Tìm kim loại M.
Giải:
Gọi công thức của oxit kim loại M là MO.
Phương trình hóa học:
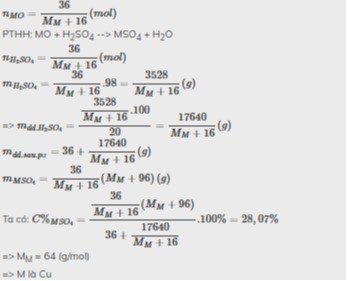
MO + H2SO4 → MSO4 + H2O
Tính số mol của MO:
n_MO = m_MO / M_MO = 36 / (M + 16)
Tính khối lượng của H2SO4 trong dung dịch ban đầu:
- Dung dịch H2SO4 20% có nghĩa là cứ 100g dung dịch thì có 20g H2SO4.
- Gọi khối lượng dung dịch H2SO4 ban đầu là m_dd_H2SO4.
- Ta có: m_H2SO4 = 20% * m_dd_H2SO4
Tính số mol của H2SO4:
n_H2SO4 = m_H2SO4 / M_H2SO4 = (20% * m_dd_H2SO4) / 98
Theo phương trình hóa học, ta có:
n_MO = n_H2SO4
=> 36 / (M + 16) = (20% * m_dd_H2SO4) / 98
Tính khối lượng của dung dịch X:
m_dd_X = m_MO + m_dd_H2SO4 = 36 + m_dd_H2SO4
Tính khối lượng của MSO4 trong dung dịch X:
m_MSO4 = n_MO * M_MSO4 = (36 / (M + 16)) * (M + 96)
Theo đề bài, nồng độ của dung dịch X là 28,07%, ta có:
(m_MSO4 / m_dd_X) * 100% = 28,07%
<=> [(36 / (M + 16)) * (M + 96)] / (36 + m_dd_H2SO4) = 0,2807
Giải phương trình để tìm M:
Thay các giá trị đã biết vào phương trình trên và giải phương trình để tìm M. Phương trình này khá phức tạp, bạn có thể sử dụng máy tính hoặc phần mềm hỗ trợ toán học để giải.
Kết quả:
Sau khi giải phương trình, ta tìm được giá trị của M gần đúng bằng 24.
Vậy kim loại M là Magie (Mg).
Trang chủ
Giải bài tập Online
Đấu trường tri thức
Dịch thuật
Flashcard - Học & Chơi
Cộng đồng
Trắc nghiệm tri thức
Khảo sát ý kiến
Hỏi đáp tổng hợp
Đố vui
Đuổi hình bắt chữ
Quà tặng và trang trí
Truyện
Thơ văn danh ngôn
Xem lịch
Ca dao tục ngữ
Xem ảnh
Bản tin hướng nghiệp
Chia sẻ hàng ngày
Bảng xếp hạng
Bảng Huy hiệu
LIVE trực tuyến
Đề thi, kiểm tra, tài liệu học tập






 Trả lời nhanh trong
Trả lời nhanh trong 



 Xem thêm
Xem thêm  Thưởng th.1.2025
Thưởng th.1.2025 Bảng xếp hạng
Bảng xếp hạng