Cho 4,6 gam natri tác dụng với nước, sau phản ứng thu được 100g dd A. Dùng 50g dd A cho tác dụng với 30g dd CuSO4 16% thu được kết tủa B và dd C
Câu 1. cho 4 ,6 gam natri td vs nước , sau p ứ thu đc 100g ddA dùng 50g dd A cho td vs 30g dd CuSO4 16% thu đc kết tủa B và dd C
a , viết PTHH
b , tính C% A , C% ddC
c , lọc kết tủa rửa sạch đem nung đến klg ko đổi thu đc chát rắn Z ,cho H2 đi qua Z nhiệt độc cao sau p ứ thu đc 2 ,08g chát rắn , tìm lg Z tham gia p ứ H2
Câu 2. cho 49 ,03 g dd HCl 29 ,78% vào bình chứa 53 ,2g 1 kloại kiềm nhóm 1 , cho bốc hơi cẩn thận dd tạo thành , trong đk có kk , thu đc bã rắn , Xđịnh kloại trong các trg hợp sau
a , bã rắn chỉ có 1 một chất , có klg 67 ,4g
b , bã rắn là hh 2chất , có klg 99 ,92g
c , bã rắn là hh 3 chất , có klg là 99 ,92g
Câu 3. cho 80g bột đồng vào 200ml dd A và 95 ,2 g chất rắn B , cho tiếp 80g bột Pb vào dd A , p ứ xong đem lọc tách đc dd D chỉ chứa một muối duy nhất và 67 ,05 g chất rắn E ,cho 40g bột kloại R (hoá trị 2 ) vào 1/10 dd D , tách đc 44 ,575 g chất rắn F , tính CM AgNO3 ? Xđịnh kloại R
Câu 4. đem 6 ,72g bột Fe cho vào dd H2SO4 đặc nóng có chứa 0 ,3 mol H2SO4 tạo ra SO2 và thu đc dd A , tính số mol từng chất trong dd A
Câu 5. cho 4 ,72g hh bột các chất Fe , FeO , Fe2O3 td vs CO dư ở nhiệt độ cao , p ứ xong thu đc 3 ,92g Fe , nếu cx ,lấy 4 ,72g hh trên ngâm vào CuSO4 dư , p ứ thu đc chất rắn nặng 4 ,96g , Xđ klg mỗi chất có trong hh
Câu 6. lấy 1 hh bột Al và Fe2O3 đem thực hiện p ứ nhiệt nhôm trong đk ko có không khí , sau p ứ kết thúc , nghiền nhỏ , trộn đều rồi chia lm 2 phần
phần 1 , tác dụng NaOH dư thu đc 8 ,96 lít H2 và còn lại phần ko tan có khối lg = 44 ,8%klg phần 1
phần 2 , đem hòa tan hết trong HCl thu đc 26 ,88 lít H2 , các p ứ xảy ra hoàn toàn
a , tính khối lg mỗi phần
b , tính klg từng chất trong hh ban đầu
11 Xem trả lời
 4.509
4.509Trang chủ
Giải bài tập Online
Đấu trường tri thức
Dịch thuật
Flashcard - Học & Chơi
Cộng đồng
Trắc nghiệm tri thức
Khảo sát ý kiến
Hỏi đáp tổng hợp
Đố vui
Đuổi hình bắt chữ
Quà tặng và trang trí
Truyện
Thơ văn danh ngôn
Xem lịch
Ca dao tục ngữ
Xem ảnh
Bản tin hướng nghiệp
Chia sẻ hàng ngày
Bảng xếp hạng
Bảng Huy hiệu
LIVE trực tuyến
Đề thi, kiểm tra, tài liệu học tập






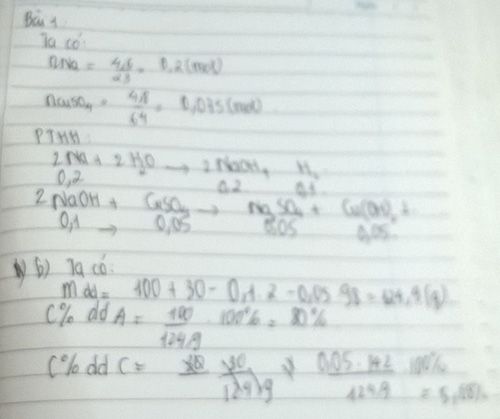
 Trả lời nhanh trong
Trả lời nhanh trong 



 Xem thêm
Xem thêm  Thưởng th.12.2024
Thưởng th.12.2024 Bảng xếp hạng
Bảng xếp hạng