a) Trong quá trình Solvay viết các phương trình hoá học của phản ứng:
- Nung vôi để cung cấp vôi sống và carbon dioxide:
CaCO3 CaO + CO2
- Tái chế ammonia từ vôi sống và dung dịch ammonium chloride.
CaO + H2O → Ca(OH)2
Ca(OH)2 + 2NH4Cl → CaCl2 + 2NH3↑ + 2H2O
Hoặc có thể viết gọn:
2NH4Cl + CaO → 2NH3 + CaCl2 + H2O
b) Quy trình Solvay đã giảm thiểu được tác động đến môi trường bằng cách quay vòng các sản phẩm trung gian (như CO2 và NH3) để tái sử dụng trong quy trình sản xuất.
Từ sơ đồ quá trình Solvay, ta có quá trình cụ thể như sau:
(1) Hoà tan NaCl vào dung dịch NH3 đặc đến bão hoà.
(2) Nung CaCO3, rồi dẫn khí thoát ra vào dung dịch bão hoà của NaCl trong NH3:
CaCO3 CaO + CO2
NaCl + NH3 + CO2 + H2O NaHCO3 + NH4Cl
(3) Do NaHCO3 ít tan hơn các muối khác nên kết tinh trước. Tách NaHCO3 ra khỏi dung dịch, nung ở nhiệt độ cao được soda:
2NaHCO3 Na2CO3 + CO2 + H2O
(4) Sản phẩm NH4Cl được chế hoá bởi vôi tôi, thu khí NH3:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O
Các khí CO2, NH3 được đưa vào sử dụng lại. NH3 được tuần hoàn trong quá trình sản xuất.
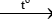
Trang chủ
Giải bài tập Online
Đấu trường tri thức
Dịch thuật
Flashcard - Học & Chơi
Cộng đồng
Trắc nghiệm tri thức
Khảo sát ý kiến
Hỏi đáp tổng hợp
Đố vui
Đuổi hình bắt chữ
Quà tặng và trang trí
Truyện
Thơ văn danh ngôn
Xem lịch
Ca dao tục ngữ
Xem ảnh
Bản tin hướng nghiệp
Chia sẻ hàng ngày
Bảng xếp hạng
Bảng Huy hiệu
LIVE trực tuyến
Đề thi, kiểm tra, tài liệu học tập







 Trả lời nhanh trong
Trả lời nhanh trong 



 Xem thêm
Xem thêm  Thưởng th.11.2024
Thưởng th.11.2024 Bảng xếp hạng
Bảng xếp hạng