Bài tập về Anken: Cho hỗn hợp hiđro và etilen có tỉ khối hơi so với hiđro là 7,5. Tính thành phần % thể tích khí mỗi khí trong hỗn hợp?
Bài 26 : Cho hỗn hợp hiđro và etilen có tỉ khối hơi so với hiđro là 7,5.
1.
Tính thành phần % thể tích khí trong hỗn hợp.
2.
Cho hỗn hợp trên vào bình kín có bột niken nung nóng làm xúc tác thì sau phản
ứng thu được một hỗn hợp khí có tỉ khối so với H2 là 9. Xác định thành phần % hỗn hợp
khí sau phản ứng.
ĐS : 50% và 50%; 20%, 40%,
40%
Bài 27 : Cho hỗn hợp X gồm anken và hiđro có tỉ khối so với heli bằng 3,33. Cho X đi
qua bột niken nung nóng thì toàn bộ anken bị hiđro hóa được hỗn hợp Y có tỉ khối so với
heli là 4.
1.
Tìm công thức phân tử của anken.
2.
Suy ra thành phần của hỗn hợp.
ĐS : C5H10, X (16%, 84%), Y (20%,
80%)
Bài 28 : Cho H2 và 1 olefin có thể tích bằng nhau qua Ni nung nóng thu được hỗn hợp A.
Biết rằng tỉ khối hơi của A đối với H2 là 23,2. Hiệu suất phản ứng hiđro hóa là 75%.
1.
Tìm công thức và gọi tên olefin.
2.
Đốt V (lít) hỗn hợp A nói trên rồi cho toàn bộ sản phẩm cháy qua 128g dung dịch
H2SO4 98% sau thí nghiệm nồng độ dung dịch H2SO4 là 62,72%. Tính V (lít) ở (đktc).
ĐS : C4H8; 22,4 lít
Bài 29 : Cho hỗn hợp A gồm 2 olefin là đồng đẳng kế tiếp nhau tham gia phản ứng hợp
nước có xúc tác thì được hỗn hợp ancol B. Cho B tác dụng với Na thu được 5,6 lít khí ở
(đktc). Mặt khác nếu đốt cháy hoàn toàn hỗn hợp A rồi cho toàn bộ sản phẩm cháy hấp
thụ hết vào nước vôi trong thì thu được 75g muối trung tính và 40,5g muối axit.
1.
xác định công thức 2 olefin.
2.
Tìm % khối lượng và thể tích từng olefin trong A.
ĐS : C2H4 và C3H6, 50%
Bài 30 : Đốt cháy hoàn toàn 0,672 lít hỗn hợp gồm hiđrocacbon và nitơ thì thu được
0,88g CO2 và 0,36g H2O. Biết khối lượng hỗn hợp là 0,84g và thể tích đo ở (đktc).
1.
Tìm công thức phân tử của hiđrocacbon.
2.
Suy ra thành phần hỗn hợp.
ĐS : C2H4, 33,33% và 66,67%
Bài 31: Cho hỗn hợp khí A ở (đktc) gồm 2 olefin. Để đốt cháy hoàn toàn 7 thể tích A cần
31 thể tích oxi ở (đktc).
1.
Xác định công thức phân tử 2 olefin. Biết rằng olefin nhiều cacbon chiếm tỉ lệ
trong 40 – 50% thể tích của A.
2.
Tìm % khối lượng các olefin trong A.
ĐS : C2H4 và C4H8; 35,5% và 64,5%
Bài 32 : Khi đốt cháy một thể tích hiđrocacbon A cần 6 thể tích oxi và sinh ra 4 thể tích
CO2. A có thể làm mất màu dung dịch brom có nối đôi và có thể kết hợp với hiđro tạo
thành một hiđrocacbon no mạch nhánh.
Xác định công thức cấu tạo của A và viết các phương trình phản ứng.
ĐS : C4H8
Bài 33 : Cho 2,24 lít một hỗn hợp khí A (đktc) gồm etan, propan, propilen sục qua dung
dịch brom dư, thấy khối lượng bình tăng thêm 2,1g. Nếu đốt cháy khí còn lại thu được
một lượng CO2 và 3,24g H2O.
1.
Tính thành phần % thể tích mỗi khí.
2.
Dẫn lượng CO2 nói trên vào bình đựng 200ml dung dịch KOH 2,6M. Hãy xác định
nồng độ M các chất trong dung dịch sau phản ứng.
ĐS : 50%, 20%, 30%, 0,65M. 1,3M
Bài 34 : Một hỗn hợp X gồm ankan A và anken B, số nguyên tử hiđro trong phân tử A
bằng số nguyên tử cacbon trong B. Khi đốt cháy 3g hỗn hợp X thì thu được 5,4g nước.
Xác định công thức phân tử A, B và tính % thể tích các khí trong hỗn hợp A.
ĐS : CH4 và C4H8; 80% và 20%
Bài 35 : Một hỗn hợp gồm H2, một ankan và một anken ( có cùng số nguyên tử cacbon
với ankan). Khi đốt 100ml hỗn hợp thu được 210ml khí CO2. Mặt khác khi nung nóng
100ml hỗn hợp với Ni thì sau phản ứng còn lại 70ml một hiđrocacbon duy nhất.
1.
Tìm công thức phân tử của ankan và anken.
2.
Định % thể tích của ankan và anken.
3.
Tính thể tích O2 cần để đốt cháy 10ml hỗn hợp (các khí đo ở cùng điều kiện)
ĐS : C3H6 và C3H8; 30%, 40%, 350ml
Bài 36 : Một hỗn hợp khí gồm nitơ và một hiđrocacbon; 0,42g hỗn hợp đó chiếm thể tích
336cm3 (đktc). Đốt cháy lượng hỗn hợp đó người ta được 0,44g CO2 và 0,18g H2O.
1.
Xác định thành phần nguyên tố của hiđrocacbon và công thức nguyên của nó.
2.
Xác định khối lượng phân tử và công thức cấu tạo.
ĐS : 85,72%, 14,28%, C2H4
Bài 37 : Đốt cháy hoàn toàn 0,25 mol khí A thu được 33g CO2 và 13,5g hơi nước.
1.
Tìm công thức phân tử và công thứ cấu tạo của A, biết rằng ở (đktc) khối lượng
riêng của A là 1,875g/l.
2.
dư.
Tính khối lượng sản phẩm tạo thành khi cho lượng chất A trên qua dung dịch brom
ĐS : C3H6 ; 50g
Bài 38 : Hai hiđrocacbon A và B đều ở thể khí, A có công thức C2xHy; B có công thức
CxH2x (trị số x trong cả 2 công thức là bằng nhau).
1.
Lập công thức phân tử A và B. Biết rằng tỉ khối của A đối với metan bằng 3,625 và
tỉ khối của B đối với He là 7. Viết công thức cấu tạo của A và B.
2.
Tính lượng sản phẩm thu được khi cho hỗn hợp trên tác dụng vừa đủ với 16g dung
dịch brom.
ĐS : x=2, y=10, 18,8g
Bài 39 : Đốt cháy hoàn toàn 0,03696 lít anken X ở 27,3oC và 1 atm, thu toàn bộ khí CO2
vào dung dịch KOH ta được 0,3g muối axit và 0,207g muối trung tính. Xác định công
thức phân tử và công thức cấu tạo của X.
ĐS : C3H6
Bài 40 : Cho 3,5g một anken tác dụng với dung dịch KMnO4 loãng thì được 5,2g sản
phẩm hữu cơ.
1.
Tìm công thức phân tử của anken.
2.
Tính thể tích oxi (đktc) cần thiết đốt cháy hết lượng anken trên.
ĐS : C5H10 và 8,4ml
Bài 41 : Một hỗn hợp hai olefin đồng đẳng kế tiếp nhau có thể tích 17,92 lít (đo ở 0oC và
2,5 atm) dẫn qua bình chứa dung dịch KMnO4 dư, thấy khối lượng bình chứa dung dịch
KMnO4 tăng 70g.
1.
Xác định công thức phân tử, viết công thức cấu tạo hai olefin.
2.
Tính % khối lượng 2 olefin trong hỗn hợp.
3.
Đốt cháy hoàn toàn thể tích trên của hỗn hợp rối cho sản phẩm vào 5 lít dung dịch
NaOH 1,8M sẽ thu được muối gì? Bao nhiêu gam?
ĐS : C3H6 và C2H4; 40% và
60%; 424g và 84g
Bài 42 : Một hỗn hợp X gồm CO và một hiđrocacbon A mạch hở. Đốt cháy hoàn toàn
1,96g hỗn hợp X được 4,84g CO2 và 1,44g H2O.
1.
Tìm dãy đồng đẳng của A.
2.
Tìm công thức phân tử của A, biết d X/H 2 = 19,6.
ĐS : CnH2n; C4H8
Bài 43 : Dẫn 2,24 lít một anken A (đktc) qua bột CuO nung nóng, khối lượng bột CuO
giảm 14,4g. Phản ứng hoàn toàn.
1.
Tìm công thức phân tử của A.
2.
Viết phương trình phản ứng trùng hợp, phản ứng của A với dung dịch KMnO4.
3.
Hỗn hợp A với một đồng đẳng B trộn theo tỉ lệ mol 1:1. Đốt cháy hoàn toàn một
thể tích hỗn hợp cần 3,75 thể tích oxi trong cùng điều kiện. Hãy gọi tên B.
ĐS : C3H6, C2H4
Bài 44 : Đốt cháy hoàn toàn a gam chất hữu cơ A cần dùng 6,72 lít O2 (đktc). Sản phẩm
cháy lần lượt qua bình P2O5 thấy bình tăng 3,6g rồi qua bình nước vôi trong thấy xuất
hiện 20g kết tủa trắng.
1.
Tính số gam a?
2.
Lập công thức thực nghiệm rồi suy ra công thức phân tử của A, biết tỉ khối hơi của
A so với nitơ là 2.
3.
Viết công thức cấu tạo có thể có, suy ra công thức đúng của A, biết A cộng với
H2O cho 1 sản phẩm duy nhất.
ĐS : 2,8;
C4H8
Bài 45 : Hỗn hợp X gồm 2 hiđrocacbon A và B (B có số cacbon lớn hơn A, A và B đều
phản ứng với dung dịch Br2). 8,96 lít hỗn hợp X tác dụng hết với nước brom cần tối thiểu
64g brom. Mặt khác, đem đốt 8,96 lít hỗn hợp X tổng số CO2 thu được là 48,4g. Hiệu số
hơi nước sinh ra của B so với A là 12,6g.
Xác định công thức phân tử của A, B.
ĐS : C3H6; C2H4
18 Xem trả lời
 8.654
8.654Trang chủ
Giải bài tập Online
Đấu trường tri thức
Dịch thuật
Flashcard - Học & Chơi
Cộng đồng
Trắc nghiệm tri thức
Khảo sát ý kiến
Hỏi đáp tổng hợp
Đố vui
Đuổi hình bắt chữ
Quà tặng và trang trí
Truyện
Thơ văn danh ngôn
Xem lịch
Ca dao tục ngữ
Xem ảnh
Bản tin hướng nghiệp
Chia sẻ hàng ngày
Bảng xếp hạng
Bảng Huy hiệu
LIVE trực tuyến
Đề thi, kiểm tra, tài liệu học tập















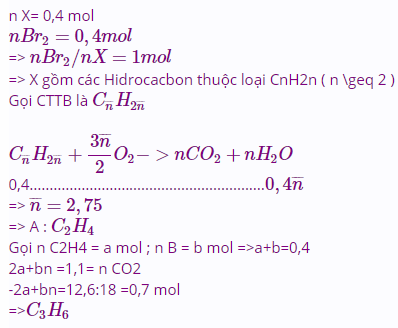

 Trả lời nhanh trong
Trả lời nhanh trong 



 Xem thêm
Xem thêm  Thưởng th.1.2025
Thưởng th.1.2025 Bảng xếp hạng
Bảng xếp hạng