TRƯỜNG THPT LÝ THÁI TỔ------------o0o-------------ĐỀ KIỂM TRA GIỮA KÌ II NĂM 2015
Môn: Hóa học lớp 10
Thời gian: 45 phút
Ngày thi 28/3/2015
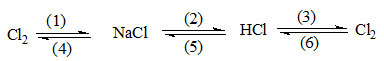
Câu 1. (3 điểm) Viết ptpư theo sơ đồ sau, ghi rõ điều kiện phản ứng (nếu có)
Câu 2. (3 điểm)
a. Cho khí SO2 vào dung dịch brom và vào dung dịch hidrosunfua. Viết ptpư xảy ra, nêu hiện tượng và xác định vai trò của SO2 trong từng phản ứng.
b. Giải thích vì sao có thể điều chế được nước clo nhưng không thể điều chế được nước flo.
c. Phân biệt 2 bình khí riêng biệt đựng oxi và ozon bằng phương pháp hóa học.
Câu 3. (3 điểm)
Đun nóng m gam hỗn hợp gồm Fe và S trong điều kiện không có oxi thu được hốn hợp X. Hòa tan hết X trong dd axit HCl dư sinh ra 6,72 lit (đktc) hỗn hợp khí Y. Cho toàn bộ khí Y vào dd NaOH dư thì thấy có 2,24 lit (đktc) khí không bị hấp thụ. Các phản ứng xảy ra hoàn toàn.
a. Viết ptpư xảy ra.
b. Tính m, biết: Fe=56; S=32.
Câu 4. (1 điểm)
Cho 1 mol mỗi chất MnO2, K2Cr2O7, KClO3 tác dụng với dd axit HCl đặc dư thì chất nào sinh ra nhiều khí clo nhất.
Đáp án đề kiểm tra giữa học kì 2 môn Hóa lớp 10Câu 1. (3 điểm)
- Viết đúng mỗi ptpư và ghi rõ đkpư được 0,5 điểm* 6 = 3 điểm.
- Không có đk, không cân bằng trừ nửa số điểm của pư đó.
Câu 2. (3 điểm)
a. (1,5 điểm)
Ptpư: SO2 + Br2 + 2H2O → H2SO4 + 2HBr (0,5đ)
(chất khử)
Htg: dd Br2 bị mất màu (0,25đ)
Ptpư: SO2 + 2H2S → 3S + 2H2O (0,5đ)
(chất oxi hóa)
Htg: dd bị vẩn đục màu vàng (0,25đ)
b. (1,0 điểm)
- Điều chế được nước clo vì clo tan nhiều trong nước nhưng chỉ một phần khí clo tác dụng với nước theo ptpư: (0,25đ)
Cl2 + H2O → HCl + HClO (0,25đ)
- Còn Flo tan trong nước thì oxi hóa hoàn toàn nước ngay ở nhiệt độ thường theo ptpư: (0,25đ)
4F2 + 4H2O → 4HF + O2 (0,25đ)
- Do đó F2 không thể tồn tại trong nước.
c. Phân biệt được O2, O3 và viết được ptpư. (0,5đ)
Câu 3. (3 điểm)
a. ptpư: (1,0 điểm)
Fe + S → FeS
0,2 <----- 0,2 <------ 0,2
FeS + 2HCl → FeCl2 + H2S
0,2 <-------------------------- 0,2
Fe + 2HCl → FeCl2 + H2
0,1 <----------------------- 0,1
H2S + 2NaOH → Na2S + 2H2O
b. (2,0 điểm)
nH2 = 2,24/22,4 = 0,1 mol
nH2S = 6,72/22,4 – 0,1 = 0,2 mol
nFe = 0,3 mol; nS =0,2
mX = (0,2+0,1).56 + 0,2.32 = 23,3 gam
Câu 4. (1 điểm)
- Viết và cân bằng 3 ptpư. (0,75đ)
- Từ đó suy ra chất tạo nhiều clo nhất là KClO3 và K2Cr2O7 (0,25đ)
Trang chủ
Giải bài tập Online
Flashcard - Học & Chơi
Dịch thuật
Cộng đồng
Trắc nghiệm tri thức
Khảo sát ý kiến
Hỏi đáp tổng hợp
Đố vui
Đuổi hình bắt chữ
Quà tặng và trang trí
Truyện
Thơ văn danh ngôn
Xem lịch
Ca dao tục ngữ
Xem ảnh
Bản tin hướng nghiệp
Chia sẻ hàng ngày
Bảng xếp hạng
Bảng Huy hiệu
LIVE trực tuyến
Đề thi, kiểm tra, tài liệu học tập












 Xem thêm
Xem thêm 
 Thưởng th.10.2024
Thưởng th.10.2024 Bảng xếp hạng
Bảng xếp hạng